
Autores: Dra. Sara Blanque, Dr. Pablo Ramallo, Dr. Matías Corroto y Dr. Federico Felder.
Desde 1986 se conoce que el yodo absorbe los rayos X. Con este hallazgo, hay una enorme cantidad de investigaciones relacionadas con su uso en la imagen médica, eficacia y efectos. No obstante ¿Qué sabemos nosotros de todo esto? Muchos reconoceremos que este medio de contraste se utiliza en las áreas de la radiología clínica y que su uso mejora la capacidad diagnóstica de las imágenes. El conocimiento de su mecanismo de acción, propiedades y fisiología, resulta necesario para extraer toda la información que genera.
El yodo es un medio de contraste positivo, hidrosoluble, es una sustancia que aumenta el coeficiente de absorción de los rayos X de diversos órganos y estructuras. En cuanto a su biodistribución, son extracelulares. Muchas estructuras presentan una atenuación similar a los rayos X, lo que dificulta su discriminación en una exploración radiológica. Si se administra una sustancia que modifique la absorción de los rayos X, se aumenta el contraste entre las distintas estructuras y será posible diferenciarlas. El estudio morfológico de las estructuras no es la única finalidad de los medios de contraste, estas sustancias también aportan información sobre la función de diversos órganos. Además, mediante los estudios dinámicos se puede valorar el comportamiento de la vascularización de numerosas lesiones.1
Este trabajo se ha elaborado con la intención de proveer un mejor conocimiento para la utilización racional de este medio de contraste en las tomografías computada (TC) de Tórax.
A continuación esquematizamos en la siguiente tabla las patologías que requieren el uso de contraste endovenoso y aquellas que no lo necesitan.

Estudio de Neoplasias Malignas
La TC es útil para el diagnóstico, estadificación, plan de tratamiento y controles posteriores a la terapéutica realizada del cáncer de pulmón y otras neoplasias primarias que comprometen al tórax, como así también a las enfermedades metastásicas.
Cuando la neoplasia tiene una atenuación similar por TC a las estructuras adyacentes (ganglios linfáticos, masas en el mediastino o pared torácica) el contraste EV puede mejorar la identificación de la lesión y delimitar sus márgenes de las estructuras vecinas.2
Estudio de las patologías vasculares torácicas.
La introducción de la Tomografía Computada Multidetectores con (TCMD) ha revolucionado la práctica radiológica, este método no invasivo, rápido cuenta con una resolución espacial submilimétrica (hasta 0.5 mm) determinada por el grosor de los detectores, que permite evaluar de manera precisa y reproducible los vasos pulmonares hasta niveles subsegmentarios (vasos de 5° y 6° orden, con un diámetro vascular mínimo de 1.5 mm).3
Para la evaluación de las patologías vasculares, la TCMD en la mayoría de los casos requiere contraste intravenoso para la delimitación de la luz del vaso.
-Tromboembolismo pulmonar:
El tromboembolismo pulmonar (TEP) es la tercera causa más común de enfermedad cardiovascular, después del infarto de miocardio y de los eventos cerebrovasculares.
Aún en nuestros días, el tromboembolismo pulmonar es considerado un reto diagnóstico, entidad con una presentación clínica inespecífica. Por este motivo, es de vital importancia el apoyo de herramientas diagnósticas no invasivas para identificar aquellos pacientes con TEP.4
Esta condición patológica, ya sea aguda o crónica, parcial o completa hace que se pongan en evidencia defectos de llenado intraluminales en las arterias pulmonares en TCMD contrastada (Fig. 1).
A pesar de que se pueden utilizar diversas modalidades de imágenes, la TC contrastada con equipos multidetector es el método de elección. La sensibilidad de la TCMD varía desde el 90 el 100%, con una especificidad que va desde el 89 al 96%5 y presenta además un valor predictivo negativo muy alto que va de desde 96,2% a-99,1%.6
El protocolo de TEP utilizado es el escaneo estándar con un barrido luego de la administración de yodo EV a 1ml/kg/peso y a una velocidad de flujo de 3-4ml/seg mediante bomba inyectora. Se coloca un ROI (Region of Interest) en el tronco de la arteria pulmonar con un pretest de 80 UH. De esta manera logramos el relleno contrastado de la luz de la arteria pulmonar y sus ramas.
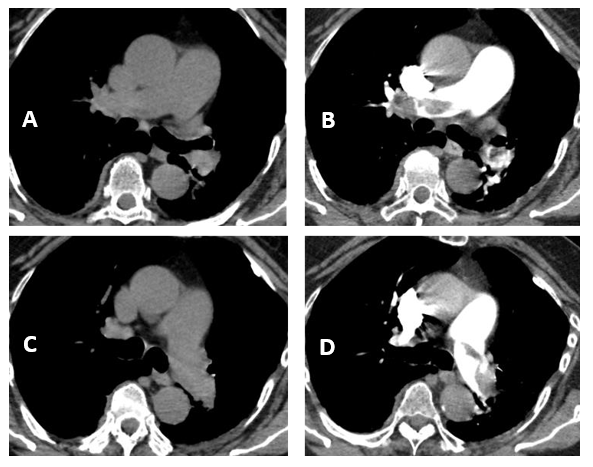
Fig. 1: Tromboenbolismo pulmonar. En las imágenes con contraste endovenoso (B y D), se puede ver con claridad los defectos de relleno intraluminales (trombosis) de la arteria pulmonar y sus ramas, que en las imágenes sin contraste endovenosos (A y C) no eran visibles.
La venografía indirecta por TC, es decir la fase venográfica del sistema profundo de las extremidades después de una angiotomografía, descrita por primera vez en 1998, es un método adyuvante a la angio–TC pulmonar que no requiere de mayor administración de contraste intravenoso y por ende no altera el protocolo de angiotomografía de las arterias pulmonares.7 Este estudio tiene una sensibilidad y especificidad similares al US Doppler de los miembros inferiores.8 La sensibilidad oscila de 71% a 100%, mientras que la especificidad es de 94% a 100%.9 Por lo tanto la US con compresión en modo doppler siendo un método no invasivo, de gran disponibilidad y económica se ha convertido en la técnica de evaluación de elección. Además la venografía indirecta por TC presenta el inconveniente de sumar dosis de radiación adicional al paciente.
-Sospecha de malformaciones vasculares pulmonares:
Las malformaciones vasculares pulmonares constituyen un espectro de anomalías con diversa presentación clínica, desde la infancia a la edad adulta, cuyos hallazgos en imagen son a menudo superponibles. Algunas de ellas son puramente vasculares como el drenaje venoso pulmonar anómalo, la hipoplasia de la arteria pulmonar o las malformaciones arteriovenosas pulmonares, otras además implican patología asociada del parénquima pulmonar, como son el secuestro broncopulmonar o el síndrome de la cimitarra.
La TCMD con contraste intravenoso es la técnica de elección para el estudio de esta patología. Permite una gran cobertura anatómica con un menor tiempo de adquisición, consiguiéndose así disminuir los artefactos respiratorios y cardiacos, y mejorando la resolución espacial del estudio. Esta técnica posibilita además la realización de reconstrucción multiplanares, volumétricas y proyecciones MIP permitiendo evaluar tamaño, ubicación, vasos aferentes y eferentes y la posibilidad de pesquisar otras posibles lesiones.13 En nuestro centro contamos con un tomógrafo de 160 canales, y el protocolo es un escaneo estándar , seguido de otro escaneo tras la administración de contraste EV a una velocidad de flujo de 4ml/seg con una inyección automática del bolo mediante un ROI pre establecido a 80 UH en la aorta ascendente, de esta manera logramos el realce vascular de interés (Fig. 2, 3, 4).
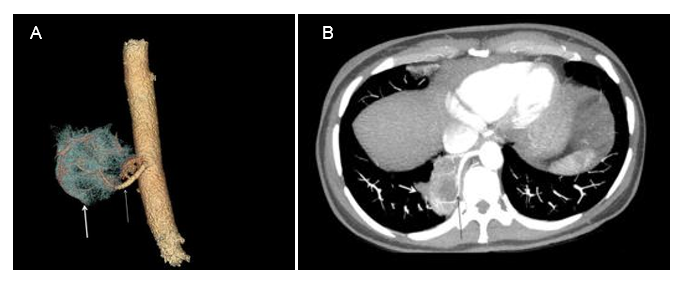
Fig. 2 A) Reconstrucción Volume Rendering (VR) de TCMD de secuestro pulmonar intralobar. Parénquima pulmonar (flecha gruesa) con vascularización arterial sistémica (flecha fina).
- B) Imagen axial de TCMD con MIP que muestra una masa pulmonar localizada en segmento basal medial de LID (flecha blanca) con aporte arterial sistémico que proviene de la pared lateral derecha de la aorta descendente (flecha negra). Secuestro pulmonar intralobar.13
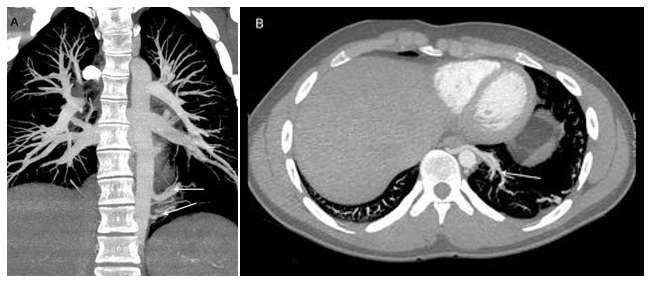
Fig. 3 Secuestro pulmonar extralobar. A. Imagen coronal MIP. Parénquima pulmonar con vascularización arterial sistémica (flechas). B. Imagen axial MIP. Drenaje venoso pulmonar anómalo del mismo segmento pulmonar a vena ácigos.13
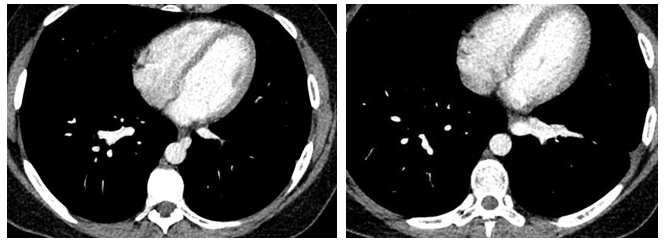
Fig. 4 Malformación arteriovenosa simple. En la imagen se observa un vaso anómalo que nace de la arteria aorta para nutrir al lóbulo inferior del pulmón izquierdo.
Infecciones Mediastinales
La mediastinitis puede ser aguda o crónica, iatrogénica o diseminarse desde la orofaringe. La TC con contraste puede ayudar a representar la infección de la pared torácica o del mediastino y en algunos casos también puede delinear la ruta de propagación.2
Como mencionamos anteriormente muchas estructuras, sobre todo las del mediastino presentan una atenuación similar de los rayos X, lo que dificultaría su discriminación. Por lo que el contraste EV con su diferente grados de absorción nos ayudara a distinguir las distintas estructuras y será posible diferenciarlas.
Nódulo pulmonar solitario
Un nódulo pulmonar solitario (NPS) se define como una lesión redondeada de menos de 3 cm de diámetro que está completamente rodeada de parénquima pulmonar sin otras anomalías. Los avances por TC helicoidal y de baja dosis con detectores múltiples, ha aumentado la tasa de detección incidental de NPS. Cuando se detecta un NPS, la TC de tórax estándar es la modalidad de elección para evaluar la morfología y el tamaño del mismo, datos que resultan indispensables para su seguimiento.
Si bien se han realizado numerosos estudios para determinar la utilidad del contraste endovenoso en la diferenciación de benignidad y malignidad de los NPS, no se obtuvieron datos ni pruebas fisiopatológicas concluyentes que permitan caracterizar uno de otro. Por lo pronto, el seguimiento se realiza con TC estándar, ayudando a diagnosticar nódulos benignos al no mostrar crecimiento o bien mostrar una disminución en su tamaño. 14
Evaluación de las enfermedades del parénquima pulmonar
La infección, inflamación y el edema del parénquima pulmonar suele estar bien representado en la TC estándar. Sin embargo, el contraste puede ser útil si hay inquietudes sobre complicaciones como la afectación de la pared torácica, donde el refuerzo con contraste puede ayudar a delimitar el alcance de las complicaciones.
La evaluación de la enfermedad pulmonar intersticial no requiere el uso de contraste intravenoso; más bien, se puede utilizar un protocolo personalizado con cortes más finos e imágenes espiratorias no contiguas para evaluar atrapamiento de la vía aérea.2
Evaluación de la Pleura
En el derrame pleural, la valoración por TC de la presencia, ubicación y extensión del derrame no requiere contraste. Sin embargo, el contraste se utiliza para evaluar sospechas de derrame de tipo exudativo conocido o empiema. Esto también ayuda a la evaluación de una malignidad primaria o metastásica de la pleura, particularmente en casos de enfermedad oculta, el engrosamiento de la pleura y su realce son de interés diagnóstico.2
Si es necesario la administración de contraste EV según lo anteriormente expuesto, el estudio se realiza con un escaneo estándar, seguido de un escaneo con inyección de contraste EV. (Fig. 5)
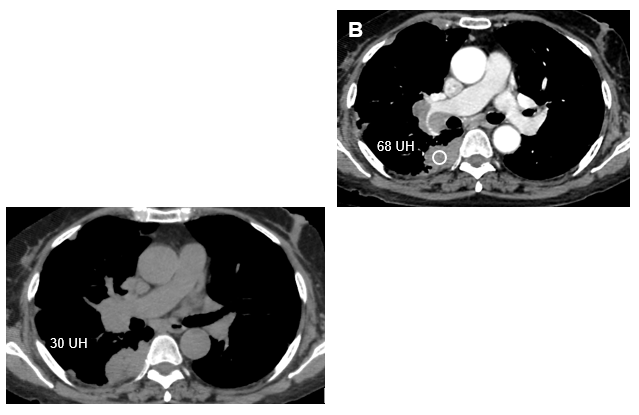
Fig 5 A) La imagen demuestra una masa hiliar derecha y un engrosamiento pleural nodular del mismo lado. B) La administración de contraste EV permite visualizar formaciones ganglionares mediastínicas aumentadas de tamaño, las que rodean a la arteria pulmonar derecha en su tercio distal y a ramas lobares. El ROI (círculo) nos muestra el aumento de la atenuación del engrosamiento pleural nodular tras la administración de contraste EV.
Evaluación de la Vía Aérea
Las enfermedades de las vías aéreas grandes, como estenosis y engrosamiento, y las enfermedades de las vías aéreas pequeñas, como la bronquiolitis, normalmente no requieren uso de contraste. Es suficiente con la valoración en técnicas de inspiración y espiración forzada.2
Referencias
- Luis Martí-Bonmatí y Yolanda Pallardó Calatayud. (2007). Medios de contraste en radiología. Sociedad Española de Radiología Médica VIII, 9-19.
- Camila Piza Purysko, Rahul Renapurkar and Michael a. bolen. (2016). When does ches t ct require contrast enhancement? Cleveland clinicjournalof medicine 83 (6) 423-426.
- Ghaye B, Szapiro D, Mastora I, et al. Peripheral pulmonary arteries: how far in the lung does multi–detector row spiral CT allow analysis? Radiology 2001; 219:629–636.
- Kuriakose J, Patel S. Acute pulmonary embolism. RadiolClin N Am 2010; 48:231–250.
- Stein, P. D., Woodard, P. K., Weg, J. G., Wakefield, T. W., Tapson, V. F., Sostman, H. D., Buckley, J. D. (2007). Diagnostic Pathways in Acute Pulmonary Embolism: Recommendations of the PIOPED II Investigators. Radiology, 242(1), 15–21. doi:10.1148/radiol.2421060971.
- CT Angiography of Pulmonary Embolism: Diagnostic Criteria and Causes of Misdiagnosis Conrad Wittram, Michael M. Maher, Albert J. Yoo, Mannudeep K. Kalra, Jo-Anne O. Shepard, and Theresa C. Mc Loud RadioGraphics 2004 24:5, 1219-1238.
- Loud PA, Grossman ZD, Klippenstein DL, et al. Combined CT venography and pulmonary angiography: a new diagnostic technique for suspected thromboembolic disease. AJR 1998; 170:951–954.
- Stein PD, Fowler SE, Goodman LR, et al. For the PIOPED II investigators. Multidetector computed tomography for acute pulmonary embolism. NEJM 2006; 354:2317–2327.
- Patel S, Kazerooni EA. Helical CT for the evaluation of acute pulmonary embolism. AJR 2005; 185:135–149.
- Winer–Muram HT, Boone JM, Brown HL, et al. Pulmonary embolism in pregnant patients: fetal radiation dose with helical CT. Radiology 2002;224:487–492.
- Huda W. When a pregnant patient has a suspected pulmonary embolism, what are the typical embryo doses from a chest CT and a ventilation/perfusion study? PediatrRadiol 2005; 35:452–453.
- Pregnancy and medical radiation. Ann ICRP 2000; 30:1–43.
- E. Sánchez Muñoz, F. M. Azcón, G. López Milena y Colab. (2012).Malformaciones vasculares pulmonares: utilidad del TCMD en su diagnóstico. Empleo de TC angiografía, reconstrucciones multiplanares, MIP y volumen rendering. SERAM .Poster S-1158.
- Xiao–Dan Ye,Jian–ding ye,Zhengyuan,Sheng dongandXiang–ShengXiao.(2012).Characterization of solitarypulmonarynodules: Use of washoutcharacteristics at contrast-enhancedcomputedtomography. OncologyLetters.3 (3): 672–676.
